Qualcuno può confrontare gli orbitali s, p, d e f in termini di dimensioni, forma ed energia?
Risposta:
questa è una bella domanda - semplice da porre, difficile da rispondere. Lo proverò....
Spiegazione:
dobbiamo impostare alcuni parametri per questa domanda. ovviamente s, p, d ed f esistono tutti a diversi livelli quantici.
ma se prendiamo il livello quantico n = 4 (il primo livello quantico in cui esistono tutte e 4 le shell secondarie - s, p, d, f -) allora potresti iniziare a disegnare alcuni confronti.
Ad esempio, potresti semplicemente usare i modelli e dire che tutti e 4 i sotto-gusci hanno approssimativamente lo stesso diametro - vale a dire che hanno tutti distanze simili dal nucleo atomico all'area principale dell'elettrone densità (o volume della massima probabilità del cloud).
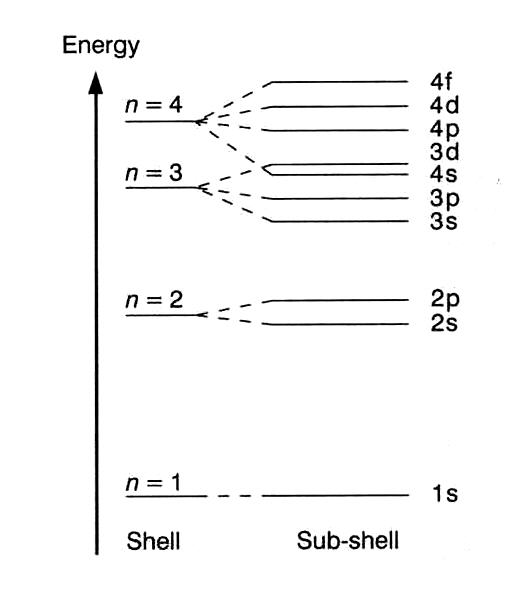
Ma l'energia di ogni sotto-shell è molto diversa - quindi il 4s è molto più stabile del 4f - motivo per cui gli atomi riempiono il sotto-guscio 4s prima del 4f. Questo è ovviamente ciò che porta al diagramma di divisione del livello quantico che potresti avere familiarità con:
 )
)
Le forme non possono essere confrontate in quanto sono tutte uniche. Puoi confrontare tutti gli orbitali s - poiché tutti hanno la stessa forma (sferica), ugualmente tutti gli orbitali p (campana muta) ecc. L'unica differenza è la dimensione - quindi 1s è una sfera piccola, 2s è una sfera più grande , Sfera 3s ancora più grande ecc.
questo potrebbe aiutare di più,
(http://hyperphysics.phy-astr.gsu.edu/hbase/Chemical/eleorb.html)

