Perché la respirazione è un processo esotermico?
Risposta:
La respirazione è un processo esotermico perché forma altamente stabile #"C=O"# legami di #"CO"_2#.
Spiegazione:
AVVERTIMENTO! Risposta lunga!
Durante la respirazione, le molecole di glucosio vengono convertite in altre molecole in una serie di passaggi.
Finiscono per diventare anidride carbonica e acqua.
La reazione generale è
#"C"_6"H"_12"O"_6 + "6O"_2 → "6CO"_2 + "6H"_2"O" + "2805 kJ"#

La reazione è esotermica perché il #"C=O"# e #"O-H"# i legami nei prodotti sono molto più stabili dei legami nei reagenti.
Energia di legame Monteverede vecchio è media energia necessaria per rompere un legame.
Alcune energie di legame sono:
#"C-C"# = 347 kJ / mol
#"C-H"# = 413 kJ / mol;
#"C-O"# = 358 kJ / mol;
#"O-H"# = 467 kJ / mol;
#"O=O"# = 495 kJ / mol;
#"C=O"# = 799 kJ / mol
Possiamo vedere il processo come rompere tutti i legami nei reagenti per separare gli atomi e quindi ricombinare gli atomi per formare i legami nei prodotti.
Una molecola di glucosio ha la formula
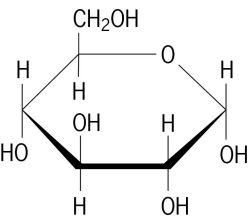
Contiene 5 #"C-C"#, 7 #"C-H"#; 7 #"C-O"#e 5 #"O-H"# obbligazioni.
il 6 #"O"_2# le molecole contengono 6 #"O=O"# obbligazioni.
I prodotti contengono 12 #"C=O"# e 12 #"O-H"# obbligazioni.
Il processo generale è
#"5C-C"color(white)(l) + "7C-H" + "7C-O" +color(red)(cancel(color(black)("5O-H"))) + "6O=O" → "12C=O" + stackrelcolor(blue)(7)(color(red)(cancel(color(black)(12))))"O-H"#
or
#underbrace("5C-C"color(white)(l) + "7C-H" + "7C-O"+ "6O=O")_color(red)("break these bonds")→ underbrace("12C=O"color(white)(l) + "7O-H")_color(red)("form these bonds")#
Le differenze energetiche in chilojoule per mole sono
#color(white)(l)"5C-C" +color(white)(l) "7C-H" + "7C-O"color(white)(l)+color(white)(l) "6O=O"color(white)(l) → "12C=O" +color(white)(l) "5O-H"#
#"5×347" + "7×413" + "7×358"+color(white)(l) "6×495"color(white)(l) → "12×799" + "7×467"#
#color(white)(l)1735color(white)(l) +color(white)(l)2891color(white)(l) +color(white)(l) 2506color(white)(l) +color(white)(ll) 2970 color(white)(m)→ color(white)(m)9588 color(white)(ll)+color(white)(l) 3269#
#color(white)(mmmmmmm)"10 102"color(white)(mmmmmmml) → color(white)(m) color(white)(mm)"12 857"#
#ΔH ≈ "(10 102 - 12 857) kJ/mol" = "-2755 kJ/mol"#
Quasi il 75% dell'energia rilasciata proviene dalla formazione della stalla #"C=O"# obbligazioni in #"CO"_2#.

