Quale tendenza nell'elettronegatività vedi mentre attraversi un periodo / riga nella tavola periodica?
Risposta:
Vedi sotto per la risposta.
Spiegazione:
Prima di continuare, voglio far capire che non è solo elettronegatività che è interessato quando attraversi un periodo o su e giù per un gruppo. Anche l'energia della ionizzazione e il raggio atomico fluttuano.
Ecco un diagramma:
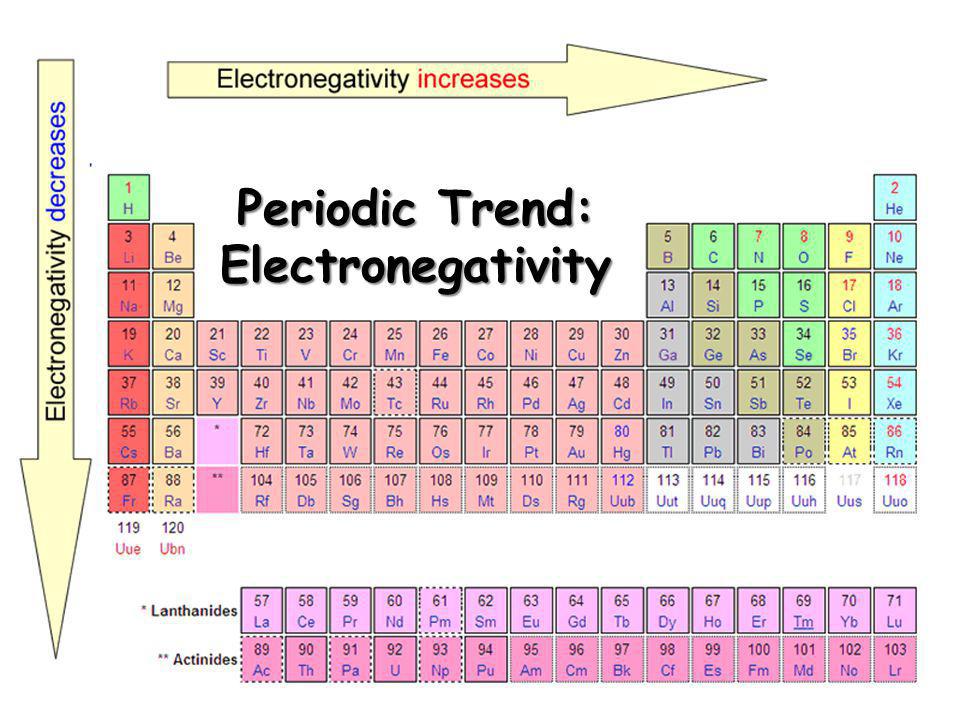
Come puoi vedere, l'elettronegatività aumenta man mano che attraversi un periodo, mentre l'elettronegatività diminuisce mentre scendi un gruppo. Tuttavia, se questo è vero (quale è), possiamo anche dire che si verificano molti altri fattori, come:
-
Mentre attraversi un periodo da sinistra a destra, l'elettronegatività aumenta, l'energia di ionizzazione aumenta e il raggio atomico diminuisce. Per aumentare l'energia, il raggio deve diminuire.
-
Mentre si va su e giù per un periodo, l'elettronegatività diminuisce, l'energia della ionizzazione diminuisce e il raggio atomico aumenta. Affinché l'energia diminuisca, il raggio deve aumentare.
-
L'elettronegatività è la forza / energia richiesta per acquisire elettroni e formare ioni negativi durante le reazioni chimiche. (credito di definizione: dal dizionario dei miei computer).
-
L'energia di ionizzazione è l'esatto contrario. La ionizzazione è la forza / energia necessaria per rimuovere gli elettroni da uno ione. Questi si sforzano di creare cationi mentre gli ioni elettronegativi di solito coinvolgono anioni (da cui la frase elettronegatività).

