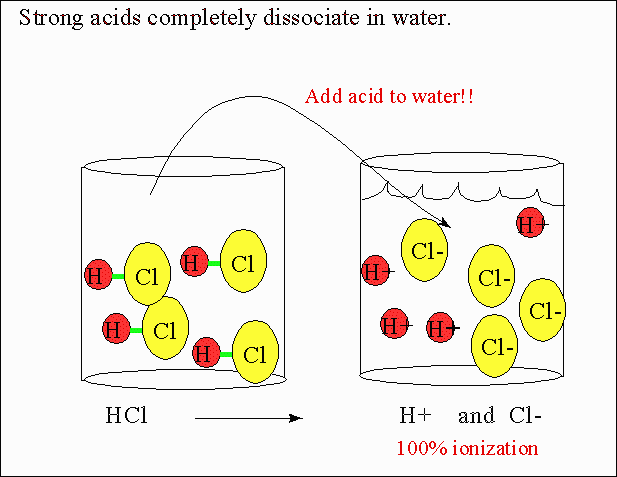
Gli acidi forti si dissociano completamente in acqua?
A tutti gli effetti pratici, gli acidi forti si dissociano completamente in acqua.
Questa è la definizione: A acido forte è un acido che si dissocia completamente in acqua.
In teoria, ogni reazione è una reazione di equilibrio. Per esempio
HCl + H₂O ⇌ H₃O⁺ + Cl⁻
K_"a" ="[H₃O⁺][Cl⁻]"/"[HCl]" = 1.55 × 10⁶
Vediamo che la posizione dell'equilibrio si trova molto a destra.
Possiamo calcolare che in 1 mol / L di HCl ci sono più di 1200 ioni H₃O for per ogni molecola di HCl non dissociato.
Per tutti gli scopi pratici, HCl è completamente dissociato in soluzione.
Gli acidi forti hanno una grande costante di dissociazione, quindi si dissociano completamente in acqua.