Perché l'etere viene usato come solvente durante le reazioni di Grignard?
Risposta:
L'etere è usato come solvente perché è aprotico e può solvatare lo ione magnesio.
Spiegazione:
Una reazione di Grignard comporta la reazione di un alchile (o alogenuro di arile) con metallo di magnesio per formare un alogenuro di alchilmagnesio.
#"R-X" + "Mg" stackrelcolor(blue)("dry ether"color(white)(X))(→) "R-MgX"#
Il dietil etere è un solvente particolarmente buono per la formazione di reagenti Grignard per due motivi.
(a) L'etere è un solvente aprotico
The #"R-Mg"# il legame è altamente polare: #stackrelcolor(blue)(δ^(-))("R"color(white)(l))-stackrelcolor (blue)(δ^+)("Mg")"X"#
Il carbonio Grignard è altamente basico e reagisce con i protoni acidi dei solventi polari come l'acqua per formare un alcano.
#stackrelcolor (blue)(δ^(-))("R"color(white)(l))"-"stackrelcolor (blue)(δ^+)("Mg")"X" + "H-OH" → "R-H" + "HO-MgX"#
L'etere non ha protoni acidi, quindi i reagenti di Grignard sono stabili nell'etere.
(b) L'etere è un ottimo agente solvante
The #"MgX"# il legame in un reagente Grignard è ionico: #"R-Mg"^+ color(white)(l)"X"^-#.
Pertanto, è difficile formare un reagente Grignard in un solvente non polare.
The #"C-O"# il legame in un etere è abbastanza polare e l'ossigeno del dipolo può solvatare e stabilizzare #"R-Mg"^+# ione.
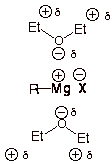
Pertanto, i reagenti Grignard sono solubili in etere.

