Qual è il momento di dipolo del tricloruro di azoto?
Il momento dipolo di NCl₃ è 0.6 D.
La struttura di Lewis di NCl₃ è
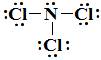
NCl₃ ha tre coppie solitarie e una coppia di legame. Questo lo rende una molecola AX₃E.
I quattro domini di elettroni gli conferiscono una geometria elettronica tetraedrica. La coppia solitaria rende la forma molecolare trigonale piramidale.
N e Cl hanno quasi esattamente le stesse elettronegatività. La differenza di elettronegatività è così piccola che i legami N-Cl non sono polari.
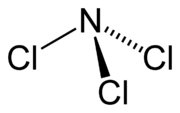
Qual è la fonte del momento dipolo? Risposta: la coppia solitaria.
Una coppia solitaria contribuirà a un momento di dipolo. I calcoli teorici mostrano che il contributo di una coppia solitaria sp³ sull'azoto può arrivare fino a 1.3 D.
Quindi è ragionevole che il momento dipolo di NCl₃ sia 0.9 D.

