Qual è la polarità del legame di CH4?
Risposta:
Il momento dipolo di a "C-H" il legame è probabilmente 0.34 D.
Spiegazione:
Spesso diciamo che a "C-H" il legame non è polare perché le elettronegatività di "C" e "H" sono così vicini l'uno all'altro.
Tuttavia, i valori sono "C = 2.55" e "H = 2.20".
La differenza corrisponde al 3% di carattere ionico, quindi a "C-H" il legame dovrebbe avere un piccolo momento di dipolo.
Dalle intensità IR sperimentali di metano, possiamo dedurlo µ_text(C-H) = "0.34 D", dirette stackrelcolor(blue)(δ⁻)("C")"-"stackrelcolor(blue)(δ⁺)("H").
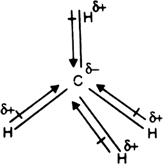
I calcoli teorici danno risultati variabili, ma la maggior parte dei valori sperimentali sono compresi tra 0.3 D e 0.4 D.

