Quali sono gli angoli di legame nell'atomo centrale di quanto segue: NSF, OF2 e IBr−2?
Risposta:
Gli angoli di legame sono leggermente inferiori a 120 °, leggermente inferiori a 109.5 ° e 180 °, rispettivamente.
Spiegazione:
NSF
La struttura di NSF is
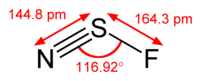
C'è una coppia sola sul N atomo, una coppia solitaria sul S atomo, e ci sono tre coppie solitarie sul F atomo.
Questo è uno AX2E molecola, quindi la geometria dell'elettrone è planare trigonale e la forma molecolare è piegata.
L'angolo di legame teorico è di 120 °, ma la repulsione delle coppie solitarie riduce l'angolo di legame a circa 117 °.
OF2
La struttura di Lewis di OF2 is

Questo è uno AX2E2 molecola, quindi la geometria elettronica è tetraedrica e la forma molecolare è piegata.
L'angolo di legame teorico è di 109.5 °, ma le repulsioni delle coppie solitarie riducono l'angolo di legame a circa 103 °.

IBr−2
La struttura di Lewis di IBr−2 is
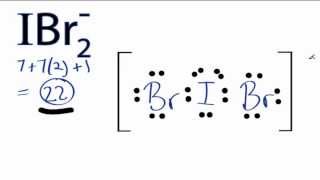
Questo è uno AX2E3 struttura, quindi la geometria dell'elettrone è bipiramidale trigonale.

Le coppie solitarie occupano le posizioni equatoriali, con il Br atomi nelle posizioni assiali.
L'angolo di legame è di 180 °.

