Come determineresti quale gas ha molecole con la massima velocità molecolare media a una certa temperatura?
Risposta:
Tutti i gas hanno la stessa velocità molecolare media a una data temperatura.
Spiegazione:
Questo è un postulato fondamentale della teoria molecolare cinetica dei gas:
L'energia cinetica media delle molecole è direttamente proporzionale alla temperatura di Kelvin.
#KE = 1/2mv^2 ∝ T#
#1/2mv^2 =kT#, Dove #k# è una costante di proporzionalità.
#v = sqrt((2kT)/m)#
Se la temperatura #T# è costante e la massa #m# di una molecola è costante, la velocità #v# deve anche essere costante.
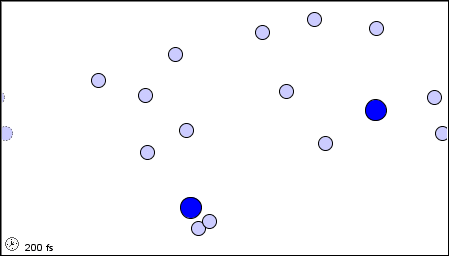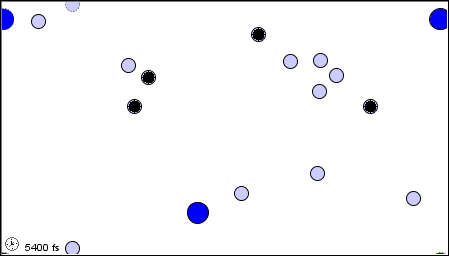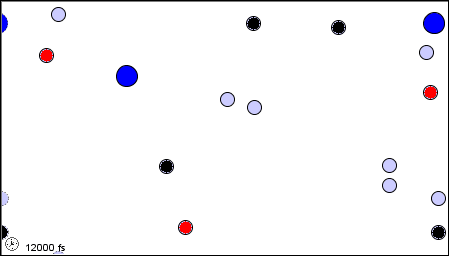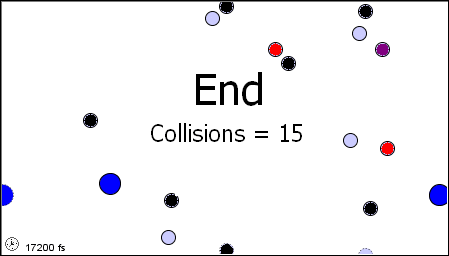
Nell'animazione sopra, le molecole di gas sono tutte alla stessa temperatura.
Le enormi molecole blu si muovono molto più lentamente delle altre e le molecole grigie si muovono più velocemente, ma hanno tutte la stessa energia cinetica media.

