Come si disegnano gli orbitali s, p, d, f?
Risposta:
Per un #s# orbitale, disegna un cerchio; per un #p# orbitale, disegna una figura otto; per un #d# orbitale, disegna un trifoglio a quattro foglie; per un #f# orbitale, vedi sotto.
Spiegazione:
An #s# orbitale è una sfera. In due dimensioni, lo disegniamo come un cerchio.
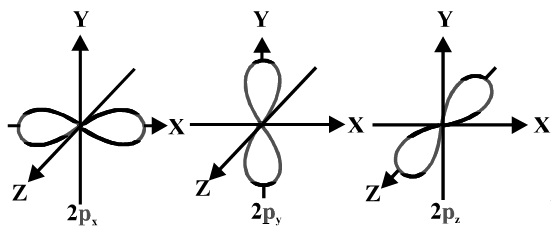
A #p# orbitale è costituito da due lobi di elettroni densità su entrambi i lati del nucleo.
Di solito disegniamo #p# orbitali come figura otto, ma dovremmo ricordare #p# gli orbitali sono molto più grassi rispetto ai nostri soliti disegni.
Quattro su cinque #d# gli orbitali sono costituiti da quattro lobi puntati verso gli angoli di un quadrato, come un quadrifoglio. Il quinto orbitale sembra un #p# orbitale con una ciambella al centro.
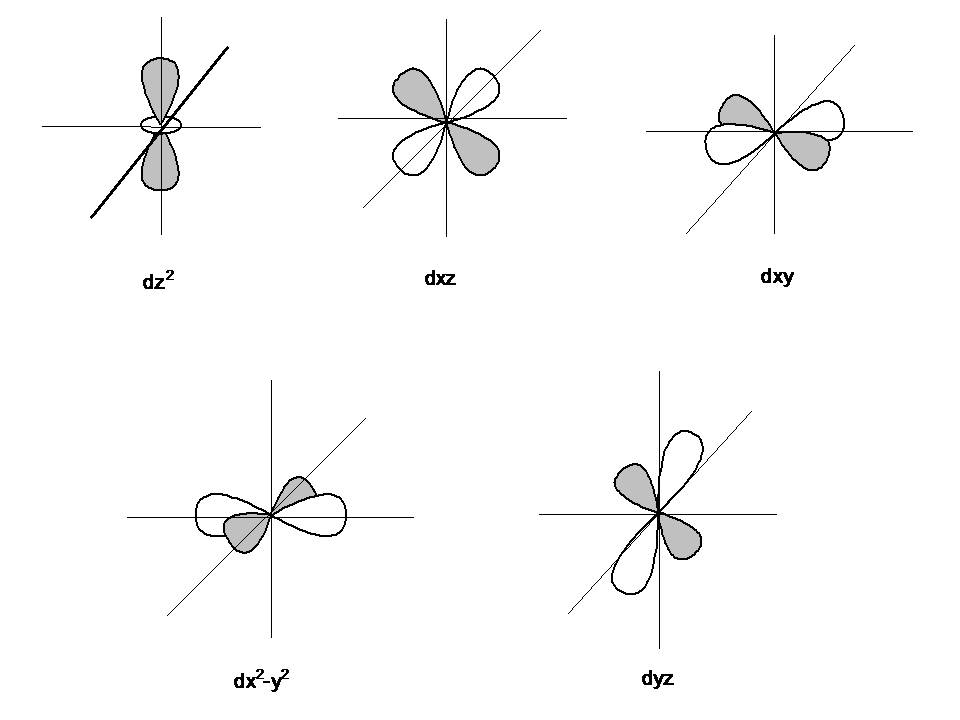
Di solito disegniamo #d# orbitali come lacrime magre che puntano in varie direzioni, ma dovremmo ricordare che i lobi sono molto più grassi rispetto al disegno.
I sette #f# gli orbitali sono forme ancora più complesse. Quelle che vediamo nei diagrammi sono combinazioni lineari di #m_l# = Da -3 a +3 orbitali. Ecco un insieme comune di combinazioni.
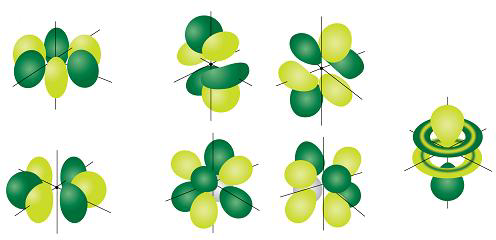
Se devi assolutamente disegnarli, puoi disegnare le forme come di seguito.

- Un orbitale sembra un #p# orbitale con due ciambelle al centro.
- Due orbitali hanno otto lobi che puntano verso gli angoli di un cubo.
- Quattro orbitali hanno sei lobi orientati su vari piani (il più facile da disegnare).

