In che modo la pressione atmosferica e l'elevazione influiscono sul punto di ebollizione?
Risposta:
- All'aumentare dell'altitudine, pressione atmosferica e il punto di ebollizione diminuisce.
Spiegazione:
-
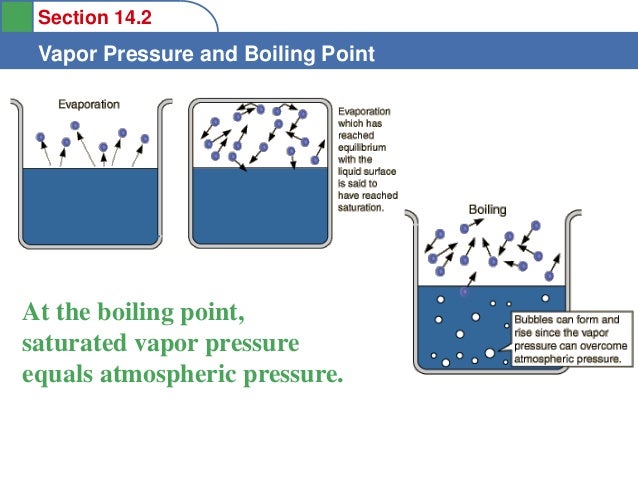
Il punto di ebollizione è il punto in cui la pressione del vapore è uguale alla pressione atmosferica.
-
In un liquido, alcune particelle hanno sempre abbastanza energia per sfuggire alla fase gassosa. Anche le particelle gassose stanno tornando al liquido.
-
The pressione del vapore è la pressione esercitata dal gas quando la quantità di particelle che escono dal liquido è uguale alla quantità di particelle che entrano nel liquido

(da facweb.bhc.edu)
- All'aumentare della temperatura, più particelle hanno energia sufficiente per sfuggire alla fase gassosa. Questo aumenta la pressione del vapore. Quando la pressione del vapore è uguale alla pressione atmosferica, il liquido bolle.
All'aumentare dell'altitudine, la pressione atmosferica diminuisce perché l'aria è meno densa ad altitudini più elevate.

Poiché la pressione atmosferica è inferiore, la pressione del vapore del liquido deve essere inferiore per raggiungere il punto di ebollizione.
Pertanto, è necessario meno calore per rendere la pressione del vapore uguale alla pressione atmosferica. Il punto di ebollizione è inferiore ad altitudine più elevata.
Ecco un video che dimostra l'effetto della pressione atmosferica sul punto di ebollizione.

